تقطیر ساده برای خالص سازی اتانول و اصول آن در آزمایشگاه شامل توضیح روش های تقطیر، کاربرد آن در جداسازی مایعات و ابزارهای مورد استفاده می باشد.
عنوان آزمایش: تقطیر
هدف: خالص سازی اتانول به روش تقطیر ساده
تئوری آزمایش
تقطیر
مقدمه:
روش های مختلفی برای جداسازی اجزای سازنده یک محلول وجود دارد که یکی از این روش ها فرایند تقطیر است. در این روش، جداسازی اجزاء یک مخلوط از روی اختلاف نقطه جوش آنها انجام می شود. تقطیر به طور کلی فرآیند جداسازی فیزیکی برش های نفتی است که اساس آن تفاوت در نقطه جوش هیدروکربن های مختلف است. به طور معمول، هر چه هیدروکربن سنگین تر باشد، نقطه جوش آن بالاتر است و هر چه هیدروکربن سبک تر باشد، سریع تر بخار می شود.
تقطیر در عمل به دو روش اصلی انجام می گیرد:
- روش اول: شامل تولید بخار از طریق جوشاندن یک مخلوط مایع و سپس میعان بخار بدون اینکه مایع دوباره به محفظه تقطیر بازگردد. در این روش هیچ مایع برگشتی وجود ندارد.
- روش دوم: در این روش، بخشی از بخار مایع شده به دستگاه تقطیر باز می گردد و در مجاورت بخاری که به طرف مبرد می رود، قرار می گیرد.
هرکدام از این روش ها می توانند به صورت پیوسته یا ناپیوسته باشند. تقطیر معمول ترین روشی است که برای تخلیص مایعات به کار می رود. در این فرایند، مایع با استفاده از حرارت تبخیر می شود و بخار مربوطه در ظرف جداگانه ای میعان کرده و محصول تقطیر به دست می آید. چنانچه ناخالصی های موجود در مایع اولیه فرار نباشند، این ناخالصی ها در باقی مانده تقطیر باقی می مانند و بدین ترتیب تقطیر ساده جسم را خالص می کند. در صورتی که ناخالصی ها فرار باشند، تقطیر جزء به جزء مورد نیاز خواهد بود.
اگر تنها یک ماده فرار باشد و اختلاف نقطه جوش این ماده با ناخالصی ها بیشتر از ۳۰ درجه سانتی گراد باشد، می توان برای جداسازی این ماده از تقطیر ساده استفاده کرد. تقطیر ساده معمولاً در جداسازی مخلوط مایعاتی که نقطه جوش آنها در محدوده ۴۰ تا ۱۵۰ درجه سانتی گراد قرار دارد، کاربرد دارد؛ زیرا در دمای بالاتر از ۱۵۰ درجه بسیاری از ترکیبات آلی تجزیه می شوند و در دمای جوش کمتر از ۴۰ درجه، مقدار زیادی از مایع در حین تقطیر از دست می رود.
تقطیر:
همان طور که گفته شد، تقطیر به فرایندی اطلاق می شود که در آن مایع تبخیر شده و بخارات آن میعان می کنند و در ظرف دیگری جمع آوری می شوند. این فرایند، روش معمولی برای خالص سازی مایعات است. در آزمایشگاه برای تخلیص مایعات چهار نوع تقطیر استفاده می شود:
- تقطیر ساده
- تقطیر در فشار کم
- تقطیر به وسیله بخار آب
- تقطیر جزء به جزء
1- تقطیر ساده
وجود ناخالصی های غیرفرار در مایع باعث کاهش فشار بخار آن می شود، زیرا وجود جزء غیر فرار، غلظت جزء اصلی فرّار را پایین می آورد و این باعث کاهش قابلیت تبخیر مایع می شود. پس از انجام تقطیر، مایع خالص در ظرف دریافت کننده باقی می ماند و ناخالصی ها در باقی مانده تقطیر باقی می مانند.
به طور کلی بخارات موجود در سطح مایع بیشتر از جسم فرّار تشکیل شده و کمتر از جسم غیر فرّار هستند (طبق قانون رائولت و دالتون). چنانچه مخلوطی از دو یا چند مایع با اختلاف نقطه جوش کافی وجود داشته باشد، می توان از تقطیر ساده برای جدا کردن آنها استفاده کرد. ابتدا مایعی که نقطه جوش کمتری دارد تقطیر می شود و سپس اجزای دیگر مخلوط به تناسب افزایش دمای جوششان تقطیر می شوند. به طور کلی، اختلاف نقطه جوش باید بیش از ۸۰ درجه سانتی گراد باشد.
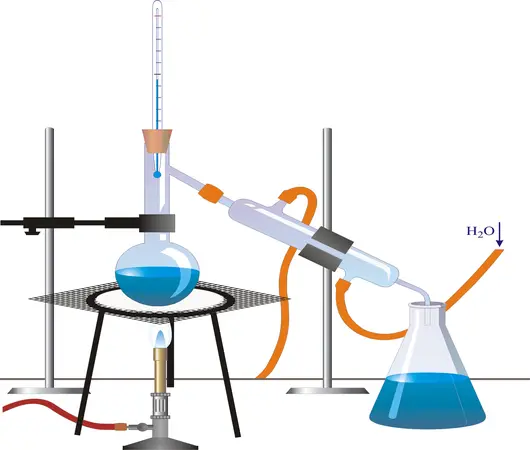
برای تقطیر ساده، به ابزارهایی نظیر بالن تقطیر (فلاسک)، مبرد، رابط، دماسنج و بالن دریافت کننده نیاز است. نحوه آماده سازی دستگاه مطابق شکل زیر است. در تقطیر یک مایع خالص، درجه حرارت دهانه خروجی رابط باید با دمای مایع جوشان در بالن تقطیر یکسان باشد، به شرطی که بالن به طور بیش از حد گرم نشود. چنانچه تنها اندازه گیری دمای جوش مدنظر باشد، می توان بدون استفاده از مبرد، دمای جوش را تعیین کرد.



























